Tirpalai - tai medžiagos dalelėms pasiskirstant kitoje medžiagoje susidarę mišiniai. Tirpalas, kuriame ištirpinta daugiausia tirpinamosios medžiagos, vadinamas sočiuoju. Kai į tirpalą įpilame dar tirpiklio, tada sakome, kad tirpalą skiedžiame. Atskiesto tirpalo koncentracija sumažėja. Paprastai tirpalą gauname kitą medžiagą ištirpinę skystyje, pavyzdžiui, kavą vandenyje, cukrų kavoje, druską jūros vandenyje, skalbiklius vandenyje, jodą spirite ir t. t. Tačiau yra ir kitokių tirpalų. Dujos gali tirpti skysčiuose (gazuotas vanduo). Daug tirpalų gaunama tirpinant vienus skysčius kituose. Kad susidarytų tirpalas, medžiaga, kuri tirpsta (tirpinamoji medžiaga), turi sąveikauti su medžiaga, kuri ją tirpina (tirpikliu).
Pavyzdžiui, kristalinis cukrus yra sudarytas iš sacharozės molekulių. Kad cukrus ištirptų, reikia energijos kristalo gardelei suardyti. Šią energiją gali suteikti tik tirpiklis. Kai tirpiklis yra vanduo, tirpinamoji medžiaga reaguoja su juo dėl vandens molekulėms būdingo poliškumo. Vandens molekulės centrinis deguonies atomas turi nedidelį neigiamą krūvį, tuo tarpu vandenilio atomai yra teigiami. Vandens molekulės yra linkusios traukti viena kitą, dėl to vanduo kambario temperatūroje yra skystas, nors dauguma mažos molekulinės masės medžiagų yra dujos. Vandens molekulės taip pat yra linkusios traukti (t. y. Panašios, tik daug stipresnės sąveikos jėgos atsiranda nepolinėse molekulėse; dėl to angliavandeniai tirpina kitus nepolinius junginius, pavyzdžiui, riebalus. Kai kurie junginiai, pavyzdžiui, etilo alkoholis, visiškai ištirpsta vandenyje ir angliavandeniuose, t. y. medžiagose, kurios netirpsta viena kitoje.
Įvairiarūšių molekulių sąveiką lengva pastebėti iš sumažėjusio medžiagos tūrio. Medžiaga netirpsta todėl, kad tirpiklis nenugali molekulių traukos jėgų. Karštas skystis paprastai geba išlaikyti kietą kūną tirpale geriau negu šaltas (dujoms ištirpintoms skystyje, galioja atvirkštinis dėsnis). Jei verdančiame vandenyje ištirpinta daugiausiai kietosios medžiagos, tai vėstant vandeniui dalis jos iškrinta (išsikristalizuoja). Jei kietos medžiagos neiškrinta, sakoma, kad tirpalas yra persotintas. Kristalizacija iš persotintų riebalų užauginami dideli kristalai. Skysčiuose tirpstančios kietos medžiagos keičia skysčių savybes. Pavyzdžiui, grynas vanduo užšąla 0° C, o verda 100° C temperatūroje. Tuo tarpu valgomosios druskos tirpalas užšąla žemesnėje negu 0° C temperatūroje.
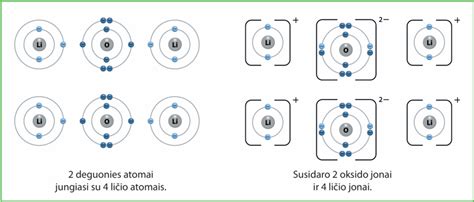
Tirpalų skirstymas
Tirpalai gali būti skirstomi pagal agregatines būsenas, ištirpusio tirpinio kiekį ir tirpinamas medžiagas. Homogeniniai tirpalai - tai vienalytės sistemos. Heterogeninė sistema - nevienalytė sistema.
Pagal ištirpusio tirpinio kiekį
Pagal ištirpusio tirpinio kiekį tirpalai skirstomi į: netirpius, mažai tirpius ir tirpius.
- Netirpios medžiagos - 100g tirpiklio ištirpsta ne daugiau, kaip 0,01g.
- Mažai tirpios medžiagos - 100g tirpiklio ištirpsta nuo 0,01g iki 3g.
- Tirpios medžiagos - 100g tirpiklio ištirpsta daugiau, kaip 3g.
Pagal tirpinamas medžiagas
Pagal tai, kokios medžiagos tirpinamos, tirpalai skirstomi į elektrolitus ir neelektrolitus. Neelektrolitai - kai tirpinamos medžiagos nedisocijuoja į jonus, o egzistuoja molekulių pavidalu, todėl yra nelaidūs elektros srovei.
Tirpalų koncentracijos skaičiavimo metodai
Tirpalo koncentracija - tai tirpale ištirpusio tirpinio kiekis. Šiame straipsnyje aptarsime tirpalų koncentracijos skaičiavimo metodus ir pateiksime praktinių uždavinių sprendimo pavyzdžių.
Procentinė koncentracija
Procentinė koncentracija (C %) rodo ištirpusios medžiagos kiekį gramais, esantį 100-te gramų tirpalo. Ji žymima C % ir yra reiškiama g/g t. y. %.
Formulė, naudojama šiai koncentracijai apskaičiuoti, yra tokia:
C % = (mmedžiagos / mtirpalo) * 100 %
Sprendžiant uždavinius su procentine koncentracija galima naudoti pateiktą formulę arba sudarant proporcijas.
Pavyzdys 1
Apskaičiuokite procentinę koncentraciją tirpalo, gauto 928 mL distiliuoto vandens ištirpinus 136 g šarmo.
Sprendimas
- Apskaičiuojame 928 mL distiliuoto vandens masę (vandens tankis yra 1,0 g/mL): m = ρ ∙ V = 1,0 g/mL ∙ 928 mL = 928 g.
- Apskaičiuojame tirpalo masę: mtirpalo = mmedžiagos + mtirpiklio = 136 g + 928 g = 1064 g.
- Apskaičiuojame tirpalo procentinę koncentraciją: C % = (136 g / 1064 g) * 100 % = 12,78 %.
Atsakymas: 12,78 %.
Pavyzdys su procentine koncentracija
Norėdami apskaičiuoti tirpalo masę arba jo tūrį, kai žinomas tankis, naudosime tankio formulę:
ρ = m / V
Taigi, žinodami tirpalo tankį ir tūrį, galime apskaičiuoti tirpalo masę: m (g) = ρ (g/mL) ∙ V (mL), arba, žinodami tirpalo masę ir tankį, galime apskaičiuoti tirpalo tūrį: V (mL) = m (g) / ρ (g/mL).
Pavyzdys 2
Kiek gramų druskos reikia paimti, norint pagaminti 0,632 L tirpalo, kurio koncentracija 53,06 % ir šio tirpalo tankis ρ = 1,210 g/mL?
Sprendimas
- Apskaičiuojame 0,632 L tirpalo masę (įrašant reikšmes į formulę, būtina suvienodinti matavimo vienetus): m (g) = ρ ∙ V = 1,210 g/mL ∙ 632 mL = 764,72 g.
- Apskaičiuojamas reikiamos druskos kiekis, 53,06% tirpalui pagaminti: 100 g tirpalo yra 53,06 g medžiagos; 764,72 g tirpalo bus x g medžiagos.
- Arba, naudojant formulę, druskos masę galima apskaičiuoti taip: x = (764,72 g * 53,06 g) / 100 g = 405,77 g.
Atsakymas: 405,77 g druskos.

Molinė koncentracija
Molinė koncentracija rodo ištirpusios medžiagos molių skaičių viename litre tirpalo. Šią koncentraciją galima apskaičiuoti ir naudojant formulę:
c = n / V
čia:
- c - molinė koncentracija (mol/L)
- n - medžiagos molių skaičius (mol)
- V - tirpalo tūris (L)
Medžiagos molinė masė
Medžiagos molinė masė (M) yra vieno molio medžiagos masė, išreikšta gramais. Ją galima apskaičiuoti pagal periodinę elementų lentelę, sudedant visų atomų atomines mases, esančias molekulėje. Pateikiami pavyzdžiai, kaip skaičiuojama medžiagų (H2O, H3PO4, Mg(OH)2, Al2(SO4)3), molinė masė.
Pavyzdžiui:
- H2O: M = 2 * 1,008 + 16,00 = 18,016 g/mol
- H3PO4: M = 3 * 1,008 + 30,97 + 4 * 16,00 = 97,994 g/mol
Molinės koncentracijos gaminimas
Išsireiškę medžiagos masę iš prieš tai pateiktos molinei koncentracijai skaičiuoti formulės:
m = c * V * M
Uždavinių pavyzdžiai
Uždavinys 1
Raskite medžiagos molinę masę, jeigu 12 l tirpalo, kurio koncentracija yra 3 mol/l, ištirpinta 1440g medžiagos.
Sprendimas
m = c * V * M
1440 = 3 * 12 * M
M = 1440 / 36 = 40 g/mol
Uždavinys 2
Vandenyje ištirpinus 11,2 g KOH, tirpalo tūris-200ml.