Katalizatorius yra molekulė, galinti pakeisti cheminės reakcijos greitį, nenaudojant minėtoje reakcijoje. Cheminės reakcijos apima energiją: pradinės molekulės, dalyvaujančios reakcijoje arba reaguojant, prasideda nuo tam tikros energijos. Papildomas energijos kiekis sugeria, kad pasiektų „pereinamąją būseną“. Vėliau energija išleidžiama su produktais. Energijos skirtumas tarp reagentų ir produktų išreiškiamas ΔG. Jei produktų energijos lygis yra didesnis nei reagentų, reakcija yra endergoninė, o ne spontaniška. Priešingai, jei produktų energija yra mažesnė, reakcija yra exergoninė ir spontaniška. Tačiau, jei reakcija yra spontaniška, tai nereiškia, kad jis pasireikš pastebimu greičiu. Reakcijos greitis priklauso nuo ΔG * (žvaigždutė reiškia aktyvinimo energiją).
Gyvojoje gamtoje vykstančių biocheminių reakcijų greitį reguliuoja biologiniai katalizatoriai - fermentai. Fermentas arba enzimas[1] - baltyminis katalizatorius, paspartinantis organizme vykstančias chemines reakcijas tūkstančius kartų. Be fermentų šios reakcijos nevyktų arba vyktų labai lėtai, ir organizmai negalėtų egzistuoti. Fermentai yra neįtikėtinai sudėtingos biologinės molekulės, daugiausia susidedančios iš baltymų. Baltymai savo ruožtu yra ilgos aminorūgščių grandinės. Viena iš ryškiausių fermentų savybių yra jų specifiškumas tikslinėje molekulėje - ši molekulė vadinama substratu.

Kas yra fermentas?
Fermentas yra baltyminis katalizatorius, paspartinantis organizme vykstančias chemines reakcijas ir sumažinantis reikalingą aktyvacijos energijos kiekį. Cheminis junginys, prie kurio prisijungia fermentas ir kurio virsmus katalizuoja vadinamas substratu. Substratas prisijungia prie fermento vietos, kuri vadinama aktyviuoju centru. Fermentai didina reakcijos greitį mažindami aktyvacijos energiją, kuri būtina reakcijai vykti. Fermentai yra baltyminiai biologiniai katalizatoriai, todėl jiems būdingos tam tikros bendrosios katalizatorių savybės ir specifinės savybės: fermentai reakcijos metu nei sunaudojami, nei pagaminami, tik didina reakcijos greitį, bet nekeičia jos pusiausvyros. Daugelis fermentų yra labai specifiški ir katalizuoja tik vieną reakciją (pvz., ureazė skaido tik šlapalą). Savybės būdingos tik fermentams: greitina tik tam tikrą cheminę reakciją ir negamina šalutinių reakcijos produktų; yra specifiški substratams. Tam tikri fermentai yra griežtai specifiški substratui, o kiti fermentai gali katalizuoti keleto junginių virsmus. Cheminės reakcijos metu substratas virsta produktu. Substrato, arba produkto, koncentracijos pokytis per laiko vienetą vadinamas cheminės reakcijos greičiu.
Fermentas sąveikauja su substratu (ar substratais), pakeičia jo struktūrą, t. y., substratą verčia į produktą. Fermentinė reakcija vyksta tik tam tikroje fermento dalyje - aktyviajame centre, kurį sudaro, formuojantis tretinei baltymo struktūrai iš skirtingų baltymo molekulės vietų, suartėjusios amino rūgščių liekanos. Fermento molekulė yra daug kartų didesnė už substrato molekulę, todėl reakcija vyksta ne visame fermento molekulės paviršiuje, bet tam tikroje srityje, vadinamoje aktyviuoju centru. Aktyviajam centrui yra būdinga erdvinė struktūra, t. y. tos aminorūgščių liekanos, kurios sudaro aktyvųjį centrą, yra išsidėsčiusios įvairiose fermento pirminės struktūros vietose. Kai, formuojantis tretinei fermento struktūrai, polipeptidinė struktūra susilanksto, šios liekanos priartėja viena prie kitos, sudarydamos aktyvųjį centrą. Fermento molekulėje gali būti vienas ir daugiau aktyviųjų centrų. Paprastai jie yra fermento paviršiaus plyšyje. Aminorūgščių liekanų skaičius įvairių fermentų aktyviosiose centruose yra skirtingas. Aktyviajame centre vidutiniškai yra apie 12-16 aminorūgščių liekanų. Aktyvusis centras sąlygiškai skirstomas į dvi sritis: substratą prijungiančią ir katalizinę sritį. Substratą prie aktyviojo centro prijungia visų rūšių silpnosios sąveikos (vandenilinis ryšys, hidrofobinė sąveika, elektrostatinė ar joninė sąveika, van der Valso sąveika), o retesniais atvejais ir kovalentinė sąveika. Fermentui prisijungus substratą, susidaro fermento-substrato kompleksas, kuris žymimas ES, čia E - fermentas, S - substratas. Substratą prijungiančios srities aminorūgščių liekanos pakreipia substrato molekulę taip, kad, veikiant katalizinės srities aminorūgščių liekanoms, ji virsta produktu.
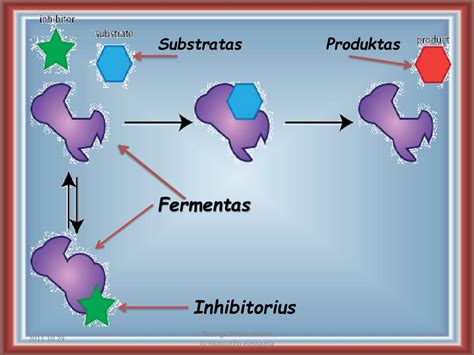
Yra pasiūlyti modeliai, aiškinantys, kaip fermentas savo aktyviajame centre sąveikauja su substrato molekule. „Spynos ir rakto“ modelis teigia, kad fermento ir jo substrato sąveika galima tik tuomet, kai substratas atitinka aktyvų centrą taip, kaip raktas spyną. Pirmąjį dar 1894 m. pasiūlė Emilis Fišeris ir jį vaizdžiai pavadino ,,spynos ir rakto” modeliu. Remiantis šiuo modeliu, fermentas gali prisijungti substratą, jei aktyviojo centro erdvinė struktūra atitinka substrato struktūrą taip, kaip raktas atitinka spyną. Tai vyksta tuo atveju, kai sąveikos su substratu metu fermento aktyviojo centro aminorūgščių liekanų erdvinė padėtis nekinta, t. y. aktyviojo centro trimatė padėtis pastovi. Antrasis fermento-substrato komplekso susidarymo modelis vadinamas „indukuoto atitikmens“ modeliu. Jis teigia, kad fermento aktyviojo centro ir substrato molekulės erdvinės struktūros yra kintančios. Aktyvusis centras įgyja formą, atitinkančią substrato molekulės formą tada, kai prie jo priartėja substrato molekulė. Keičiantis erdvinei fermento struktūrai, aktyviojo centro aminorūgščių liekanos užima tokią padėtį, kuri palankiausia ES kompleksui susidaryti ir substrato molekulę pakreipti katalizinių grupių link. Aktyviojo centro aminorūgščių liekanos keičia elektroninio debesies tankį prijungto substrato molekulėje, todėl sumažėja pereinamosios būsenos standartinė laisvoji energija.
Fermentų charakteristikos
Fermentai egzistuoja keliomis formomis. Kai kurie iš jų susideda tik iš baltymų, o kitose - ne baltymai, vadinami kofaktoriais (metalais, jonais, organinėmis molekulėmis ir kt.). Prie fermento baltyminės dalies (apofermento), kad jis galėtų atlikti savo funkcijas, aktyviajame centre prijungiama nebaltyminė dalis - kofaktorius. Taigi, apoenzimas yra fermentas be jo kofaktoriaus, o apoenzimo ir jo kofaktoriaus derinys vadinamas holoenzimu. Visi sudėtiniai fermentai ir kai kurie paprastieji yra aktyvūs tik tada, kai yra prisijungę tam tikras nebaltymines molekules arba jonus. Tokios fermentinei katalizei būtinos molekulės arba jonai vadinami kofaktoriais. Kofaktoriai prijungiami tam tikroje aktyviojo centro vietoje. Apofermentas ir kofermentas pavieniui yra neaktyvūs. Kofermentai dažniausiai yra vandenyje tirpūs, pvz., B grupės vitaminai (B1, B2, B6, B12), folinė rūgštis. Kad fermentai būtų aktyvūs, vitaminų maiste turi būti pakankamai.
Jie yra žymiai didelio dydžio molekulės. Tačiau tik nedidelė fermento vieta tiesiogiai dalyvauja reakcijoje su substratu, ir šis regionas yra aktyvi vieta. Kai reakcija prasideda, fermentas yra sujungtas su jo substratu, nes raktas yra sujungtas su jos užraktu (šis modelis yra tikrojo biologinio proceso supaprastinimas, bet padeda iliustruoti procesą).
Visos cheminės reakcijos, kurios atsiranda mūsų organizme, yra katalizuojamos fermentų. Iš tiesų, jei šių molekulių nebūtų, mes turėtume laukti šimtus ar tūkstančius metų, kad reakcijos būtų užbaigtos. Todėl fermentinio aktyvumo reguliavimas turi būti kontroliuojamas labai specifiniu būdu.
Fermentų nomenklatūra ir klasifikacija
Kai matome molekulę, kurios pavadinimas baigiasi -aze, galime būti tikri, kad tai yra fermentas (nors yra šios taisyklės išimčių, pvz., Trippsinas). Tai yra konvencija, skirta nurodyti fermentų pavadinimą.
Fermentai pagal katalizuojamos reakcijos tipą skirstomi į 6 klases. Yra šeši pagrindiniai fermentų tipai: oksidoreduktazės, transferazės, hidrolazės, liazės, izomerazės ir ligazės; atsako už: redokso reakcijas, atomų perkėlimą, hidrolizę, dvigubų ryšių pridėjimą, molekulių izomerizaciją ir rišimąsi. 6) ligazės (sintetazės), katalizuojančios sintezės reakcijas (naujų cheminių junginių susidarymas).
| Klasė | Katalizuojama reakcija |
| Oksidoreduktazės | Oksidacijos - redukcijos procesai |
| Transferazės | Atomų perkėlimas |
| Hidrolazės | Hidrolizė |
| Liazės | Dvigubų ryšių pridėjimas |
| Izomerazės | Molekulių izomerizacija |
| Ligazės (sintetazės) | Sintezės reakcijos |
Kaip veikia fermentai?
Skyriuje apie katalizę paminėjome, kad reakcijos greitis priklauso nuo ΔG * vertės. Kuo didesnė ši vertė, tuo lėtesnė ir lėtesnė reakcija. Fermentas yra atsakingas už minėto parametro mažinimą, taip padidindamas reakcijos greitį. Skirtumas tarp produktų ir reagentų išlieka identiškas (fermentas jo nedaro), kaip ir jo pasiskirstymas. Fermentas palengvina perėjimo būsenos formavimąsi.
Cheminė reakcija vyksta savaime, kai susidariusių produktų laisvoji energija yra mažesnė už substratų energiją. Norint pradėti cheminę reakciją reikia aktyvinti reaguojančias molekules-turi susidaryti pereinamoji būsena. Cheminės reakcijos greitis priklauso nuo energijos barjero, kurį turi įveikti produktu virstantis substratas.
Fermentų veikimo galima suskaidyti į 3 stadijas: substrato susijungimas su fermentu; katalizė (skaidymas); reakcijos produktų atsiskyrimas. Prie substrato jungiasi aktyvusis fermento centras, kuris turi katalizinę (veikimo) ir reguliacinę dalis. Jo molekulės išsidėsto erdvėje taip, kad susiformuoja niša, į kurią patekęs substratas yra suskaidomas. Dažnai fermentai veikia susibūrę į grupes. Fermentai katalizuoja reakciją ištirpę arba prisijungę prie membranų.
Biologinių katalizatorių (fermentų) ir cheminių katalizatorių skirtumas
Yra cheminio pobūdžio katalizatoriai, kurie, kaip ir biologiniai, didina reakcijų greitį. Tačiau yra didelių skirtumų tarp abiejų molekulių tipų.
Reakcijos, kurias katalizuoja fermentai, vyksta greičiau
Pirma, fermentai sugeba padidinti reakcijų greitį maždaug 10 kartų6 iki 1012. Cheminiai katalizatoriai taip pat didina greitį, tačiau tik kelis dydžius.
Dauguma fermentų veikia fiziologinėmis sąlygomis
Kadangi biologinės reakcijos vyksta gyvų būtybių viduje, jų optimalios sąlygos apsiriboja fiziologinėmis temperatūros ir pH vertėmis. Kita vertus, chemikai reikalauja drastiškų temperatūros, slėgio ir rūgštingumo sąlygų.
Specifiškumas
Fermentai yra labai specifiniai reakcijose, kurias jie katalizuoja. Daugeliu atvejų jie dirba tik su vienu substratu arba keliais. Šis specifiškumas taip pat taikomas gaminamų produktų tipui. Cheminių katalizatorių substratų diapazonas yra daug platesnis.
Jėgos, lemiančios fermento ir jo substrato sąveikos specifiškumą, yra tos pačios, kurios lemia to paties baltymo konformaciją (Van der Waals sąveika, elektrostatinės, vandenilio jungtys ir hidrofobiniai).
Fermentinis reguliavimas yra tikslus
Galiausiai, fermentai turi didesnį reguliavimo pajėgumą ir jų aktyvumas priklauso nuo skirtingų medžiagų koncentracijos ląstelėje. Tarp reguliavimo mechanizmų randame allosterinę kontrolę, kovalentinį fermentų modifikavimą ir sintezuojamo fermento kiekio kitimą.
Fermentų aktyvumas priklauso nuo terpės rūgštingumo (pH), temperatūros, vandenilio jonų koncentracijos, substrato koncentracijos. Fermentų aktyvumas yra reguliuojamas, t. y. jis priklauso nuo tam tikrų junginių kiekio ląstelėje.
Fermentai, kaip visi katalizatoriai, reakcijos metu nėra nei sunaudojami, nei pagaminami. Jie nekeičia reakcijos pusiausvyros, o tik padidina reakcijos greitį. Tik fermentams būdinga tai, kad jie sąveikauja griežtai tik su tam tikrais substratais, yra stereospecifiški. Fermentas yra aktyvus tik tam tikroje temperatūroje. Temperatūrai didėjant fermentas ima denatūruoti ir nebeatlieka savo funkcijos. Reakcijos greitis priklauso nuo aktyvių fermentų kiekio.
Fermentai (atnaujinta)
Fermentai naudojami kaip vaistiniai preparatai, kaip reagentai ar biocheminiai rodikliai diagnozei nustatyti. Dažniausiai vartojami gydyti ligoms, kuriomis susergama dėl fermentų nepakankamumo. Dažniausiai vartojami virškinimo fermentai ir audinių fermentai. Svarbiausi ir dažniausiai vartojami audinių fermentai yra lidazė ir ronidazė. Juose yra pagrindinio audinių fermento hialuronidazės. Vartojami gydyti nuo sklerodermijos ir kai kurių kitų ligų, kuriomis sergant išveša jungiamasis ir surandėja kiti organizmo audiniai. Itin aktyvus audinių fermentas yra penicilinazė. Kaip priešvėžinis vaistas vartojamas fermentas a-asparaginazė.
Žmogaus organizme yra aptikta daugiau nei 5 tūkst. 22 skirtingų tipų fermentų, kurių daugelis gaminama kasoje.
tags: #kuo #skiriasi #fermentas #nuo #katalizatoriaus